Sommaire
La paresthésie consécutive à un traumatisme mécanique est l'une des causes les plus fréquentes des troubles sensitifs du nerf alvéolaire inférieur. La présente étude de cas décrit le traitement chirurgical d'une paresthésie causée par une compression à l'intérieur du canal mandibulaire. La cause de la compression – un instrument brisé laissé dans la bouche de la patiente lors d'un traitement endodontique fait antérieurement – a été découverte par des radiographies de routine et une tomodensitométrie. La paresthésie s'est rapidement dissipée après l'extraction chirurgicale du corps étranger. Ce cas souligne le risque qu'un facteur mécanique iatrogène cause une paresthésie.
Introduction
La paresthésie buccale est décrite comme une sensation de picotements dans la lèvre inférieure, qui peut être continue ou intermittente1. Divers termes sont utilisés par les patients pour décrire cette sensation : chaleur, froid, brûlure, piqûre, fourmillements, picotements, engourdissement, démangeaisons et formication1-5. La paresthésie peut être associée à un traumatisme mécanique, à une compression, à un effet neurotoxique ou à une brûlure thermique1,6.
L'étude de cas qui suit décrit les résultats d'imagerie et le traitement chirurgical d'une patiente atteinte d'une paresthésie due à une compression.
Étude de cas
Une femme de 23 ans s'est présentée dans un cabinet privé en septembre 2009 pour une douleur des côtés gauche et droit de la bouche qui était due à une pulpite irréversible des dents 26 et 36. La femme n'avait jamais fumé ni consommé d'alcool et elle n'avait pas d'antécédents personnels ou familiaux pertinents. L'examen clinique intrabuccal a révélé une fracture de l'obturation de la dent 37, ainsi que plusieurs caries dentaires et une gingivite importante.
Une radiographie rétroalvéolaire a montré la présence d'un instrument endodontique brisé dans la racine mésiale de la dent 37. La radiographie a aussi montré une parodontite apicale chronique de la racine distale, ainsi qu'une radioclarté qui était très près du nerf alvéolaire inférieur et qui semblait en contact direct avec le nerf (ill. 1). La patiente a été questionnée sur son traitement endodontique antérieur. Elle se rappelait que le traitement avait été effectué en 2003 et qu'elle avait depuis ressenti parfois des engourdissements dans la lèvre gauche et une petite partie du menton. Elle a aussi mentionné des picotements dans la gencive vestibulaire et indiqué que ces symptômes étaient plus marqués le matin et lorsqu'elle était stressée. Comme ces engourdissements inquiétaient la patiente, celle-ci avait consulté un neurologue à ce sujet. Nous n'avons pas évalué la sensibilité des tissus mous de la patiente durant notre consultation, car les symptômes de la paresthésie n'étaient alors pas apparents.
En raison de la proximité du corps étranger avec le nerf alvéolaire inférieur, une tomodensitométrie a été réalisée pour déterminer l'emplacement et les dimensions de l'objet et sa relation par rapport aux structures anatomiques. La tomodensitométrie a montré que l'instrument endodontique brisé était en contact direct avec le canal mandibulaire. L'instrument sortait d'environ 3 mm de l'apex de la dent et de la radioclarté périapicale (ill. 2 et 3).
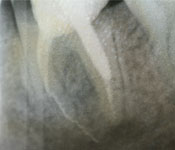
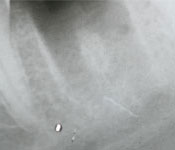
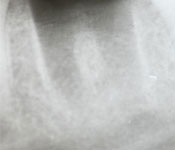
Ill. 1: Radiographies rétroalvéolaires de la dent 37, respectivement avant, pendant et après la chirurgie.
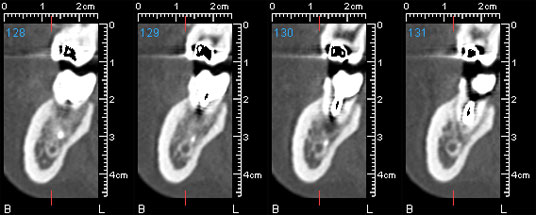 Ill. 2: Tomodensitométrie transversale buccolinguale montrant un instrument endodontique brisé en contact direct avec le canal alvéolaire inférieur.
Ill. 2: Tomodensitométrie transversale buccolinguale montrant un instrument endodontique brisé en contact direct avec le canal alvéolaire inférieur.
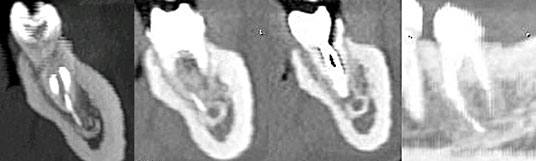 Ill. 3: Reconstructions multiplanaires de la dent 37, montrant l'instrument endodontique et la radioclarté périapicale en contact direct avec le canal alvéolaire inférieur.
Ill. 3: Reconstructions multiplanaires de la dent 37, montrant l'instrument endodontique et la radioclarté périapicale en contact direct avec le canal alvéolaire inférieur.
Il a été proposé à la patiente d'extraire la dent 37 et de retirer l'instrument brisé. La patiente a été informée des complications qui pourraient survenir durant et après la chirurgie. La dent a été sectionnée et les racines distale et mésiale ont été retirées séparément. La zone a été nettoyée à fond avec une curette, jusqu'à ce que le petit fragment de l'instrument brisé puisse être retiré (ill. 4). La lésion radioclaire périapicale associée à la racine distale a aussi été nettoyée à la curette.
 Ill. 4 : Photographie de l'instrument endodontique brisé.
Ill. 4 : Photographie de l'instrument endodontique brisé.
Afin de prévenir l'œdème et la douleur après la chirurgie, nous lui avons prescrit un antibiotique (amoxicilline 1 g, 1 comprimé 2 fois par jour pendant 8 jours), un corticostéroïde (méthylprednisolone 16 mg, dose décroissante de 4 comprimés le premier jour à 1 comprimé le quatrième jour), un analgésique (paracétamol 1 g, 1 comprimé 2 fois par jour pendant 3 jours) et un complexe vitaminique B [Neurobion (Merck KGaA, Darmstadt, Allemagne), 1 comprimé, 1 fois par jour pendant 2 mois]. Nous lui avons également recommandé de se rincer la bouche avec du gluconate de chlorhexidine 0,2 % 3 fois par jour pendant 15 jours. Huit jours après la chirurgie, la patiente a indiqué que les engourdissements avaient cessé.
Discussion
Il existe 4 causes principales de paresthésie buccale. La première – les traumatismes mécaniques – résulte principalement d'une surinstrumentation au-delà de l'apex qui cause des lésions du nerf alvéolaire inférieur normalement associé aux deuxièmes molaires6. La deuxième cause (phénomène de compression) peut se produire lorsque des matériaux d'obturation ou des instruments endodontiques sont présents dans le canal alvéolaire inférieur3,7. La troisième (effets neurotoxiques) est liée aux solutions qui sont utilisées pour nettoyer le canal radiculaire ou aux scellants6. Enfin, la quatrième cause est la brûlure thermique. L'hyperextension et la surinstrumentation sont les facteurs étiologiques les plus souvent associés à la paresthésie consécutive à un traitement endodontique orthograde (classique)8.
La paresthésie dentaire peut se manifester en association avec un traitement de canal, bien qu'elle ne se limite pas à ce contexte. Par exemple, comme l'indiquent Cohenca et Rotstein9, des tests visant à déceler la présence de pulpe nécrosée dans les dents adjacentes devraient être faits chez certains patients qui présentent des symptômes de paresthésie.
Des examens devraient aussi être faits pour découvrir d'autres facteurs localisés comme une fracture mandibulaire, des lésions expansives ou compressives (y compris des tumeurs malignes), des dents incluses, des lésions iatrogènes consécutives à l'extraction d'une dent, l'administration d'un anesthésique par injection, des implants ou des séquelles d'une chirurgie orthodontique2,4,9. Les lésions iatrogènes sont la cause la plus courante des troubles sensitifs du nerf alvéolaire inférieur5.
Il semble y avoir une corrélation entre, d'une part, la durée, l'origine et l'importance du traumatisme et, d'autre part, le pronostic de la paresthésie. Ainsi, plus l'irritation mécanique ou chimique dure longtemps, plus la dégénérescence de la fibre nerveuse sera importante et plus le risque sera grand que la paresthésie devienne permanente1.
Seddon10 a décrit 3 stades de lésions nerveuses basés sur la gravité de la lésion, le pronostic et le délai de rétablissement: la neurapraxie, l'axonotmésis et la neurotmésis. La neurapraxie est due principalement à la compression du nerf; le rétablissement est complet et il survient après quelques heures ou quelques jours. L'axonotmésis se définit comme une diminution de la continuité nerveuse; le rétablissement prend plusieurs mois, mais il est incomplet. Enfin, la neurotmésis est le stade le plus grave des lésions des nerfs périphériques. Il ne peut y avoir rétablissement complet, mais un rétablissement partiel est possible si une réparation primaire est effectuée.
La compression est le principal mécanisme qui cause une atteinte des nerfs périphériques. La compression de l'artère qui irrigue un nerf cause une augmentation de la perméabilité vasculaire, un œdème et une ischémie et réduit ainsi l'apport d'oxygène au nerf5. La réaction classique à la neurapraxie est la paresthésie, mais il peut aussi y avoir axonotmésis si la compression dure suffisamment longtemps. En pareils cas, le rétablissement peut prendre jusqu'à un an.
Selon l'étude anatomique réalisée par Tillota-Yasukawa et coll.1, l'os spongieux dans la région molaire contient de nombreuses vacuoles, et aucun os cortical ne protège le pédicule. Dans 8 des 40 cas examinés par ces auteurs, l'os spongieux était légèrement plus dense autour du canal, mais les perforations demeuraient nombreuses, empêchant ainsi une protection efficace du nerf. Ces auteurs ont également déterminé qu'il y avait moins de 1 mm entre le nerf alvéolaire inférieur et l'apex des deuxièmes et troisièmes molaires. Littner et coll.11 présentent toutefois des données contraires, selon lesquelles le bord supérieur du canal mandibulaire est habituellement situé à une distance de 3,5 à 5,4 mm sous l'apex des premières et deuxièmes molaires et le canal mandibulaire n'est jamais situé près de l'apex des premières et deuxièmes molaires. Ces dernières observations ont été corroborées par Knowles et coll.3 qui ont confirmé que le canal mandibulaire est cribriforme, et non solide. Lorsqu'un traitement endodontique doit être réalisé sur la deuxième molaire, une évaluation radiographique rigoureuse devrait être faite pour estimer cette distance12.
Durant le traitement endodontique, la radiographie devrait être prise en utilisant des limes de la longueur de travail appropriée pour éviter les perforations et les lésions du nerf alvéolaire inférieur. Si un instrument endodontique cause des lésions mécaniques du nerf inférieur alvéolaire, celui-ci peut être réparé par un processus de cicatrisation qui causera une paresthésie immédiate mais temporaire1,13. La préparation étendue qu'exige un traitement endodontique entraîne la disparition de la constriction apicale, ce qui permet le passage des produits d'irrigation et des matériaux d'obturation et cause ainsi des lésions nerveuses de type chimique ou mécanique.
Il peut également y avoir surinstrumentation si un granulome est présent à l'apex. Ce type de lésion forme une zone ostéolytique constituée d'os moins dense dans la région périapicale, ce qui peut permettre le passage des instruments au-delà de l'apex et ainsi endommager le nerf alvéolaire inférieur13.
Dans la mesure du possible, le traitement devrait commencer par l'élimination de la cause immédiate. L'inflammation, l'œdème, l'hématome ou l'infection doivent être maitrisés2 afin de prévenir les dommages irréversibles comme la fibrose réactive et le névrome2,5,13,14. Divers médicaments peuvent être administrés, notamment des antibiotiques, des anti-inflammatoires non stéroïdiens et des corticostéroïdes, des enzymes protéolytiques (pour désagréger le coagulum) et de la vitamine C (pour son action antioxydante)2. Gatot et Tovi15 ont suggéré d'administrer de la prednisolone pour réduire la durée du problème, prévenir la fibrose et atténuer la gravité des séquelles. Aucun consensus n'a toutefois pu être établi quant au type ou à la dose de stéroïdes appropriés ou à la durée du traitement. Un traitement chirurgical est indiqué lorsque le nerf a été sectionné, qu'un corps étranger cause une compression ou qu'il y a néoplasie nerveuse ou anesthésie ou paresthésie persistante2. Le principal avantage de la chirurgie durant les premiers stades de la paresthésie tient au rétablissement du système microvasculaire du nerf qui permet la régénération nerveuse. Les résultats de la décompression chirurgicale sont toutefois imprévisibles et la chirurgie comporte certains risques, notamment le sectionnement du nerf ou la formation d'une autre lésion qui pourrait causer une anesthésie complète14. Girard16 recommande la prudence durant l'exécution de toute procédure susceptible de causer des lésions nerveuses.
Plusieurs médicaments visant à promouvoir le rétablissement à la suite de lésions nerveuses ont été évalués, notamment les vitamines B1, B6 et B12 (composition du complexe vitaminique B qui a été administré à la patiente de l'étude de cas). Bien que ces substances améliorent la régénération des nerfs périphériques dans des modèles animaux, aucune donnée scientifique ne corrobore ces effets chez les humains17-19.
Dans le cas présenté ici, plusieurs facteurs ont sans doute contribué à la paresthésie, notamment l'instrument endodontique brisé, la lésion périapicale radioclaire en contact direct avec le canal mandibulaire et les réactions inflammatoires connexes. La résolution rapide de la paresthésie laisse croire que celle-ci était due à la compression du nerf alvéolaire inférieur, un phénomène compatible avec une neurapraxie.
En raison de l'étroite relation anatomique entre les deuxièmes molaires et le nerf alvéolaire inférieur, un examen clinique et radiographique minutieux devrait toujours être fait avant un traitement endodontique de ces dents, pour prévenir les lésions iatrogènes du type décrit dans cet article. Les dentistes devraient également connaître les caractéristiques anatomiques du canal mandibulaire (c.-à-d. cribriforme plutôt que solide), ainsi que les conséquences d'une surinstrumentation.
LES AUTEURS
Références
- Tilotta-Yasukawa F, Millot S, El Haddioui A, Bravetti P, Gaudy JF. Labiomandibular paresthesia caused by endodontic treatment: an anatomic and clinical study. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2006;102(4):e47-59. Epub 2006 Aug 10.
- Di Lenarda R, Cadenaro M, Stacchi C. Paresthesia of the mental nerve induced by periapical infection: a case report. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2000;90(6):746-9.
- Knowles KI, Jergenson MA, Howard JH. Paresthesia associated with endodontic treatment of mandibular premolars. J Endod. 2003;29(11):768-70.
- Morse DR. Endodontic-related inferior alveolar nerve and mental foramen paresthesia. Compend Contin Educ Dent. 1997;18(10):963-8, 970-3, 976-8 passim; quiz 98.
- Scolozzi P, Lombardi T, Jaques B. Successful inferior alveolar nerve decompression for dysesthesia following endodontic treatment: report of 4 cases treated by mandibular sagittal osteotomy. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2004;97(5):625-31.
- Pogrel MA. Damage to the inferior alveolar nerve as the result of root canal therapy. J Am Dent Assoc. 2007;138(1):65-9.
- Fanibunda K, Whitworth J, Steele J. The management of thermomechanically compacted gutta percha extrusion in the inferior dental canal. Br Dent J. 1998;184(7):330-2.
- Ingle JI, Bakland LK. Endodontics. 4th ed. Baltimore: Williams & Wilkins; 1994.
- Cohenca N, Rotstein I. Mental nerve paresthesia associated with a non-vital tooth. Dent Traumatol. 1996;12(6):298-300.
- Seddon HJ. Three types of nerve injury. Brain. 1943;66(4):237-88.
- Littner MM, Kaffe I, Tamse A, Dicapua P. Relationship between the apices of the lower molars and mandibular canal--a radiographic study. Oral Surg Oral Med Oral Pathol. 1986;62(5):595-602.
- Köseoglu BG, TanrIkulu S, Sübay RK, Sencer S. Anesthesia following overfilling of a root canal sealer into the mandibular canal: a case report. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2006;101(6):803-6. Epub 2006 Jan 4.
- Gallas-Torreira MM, Reboiras-Lopez MD, Garcia-Garcia A, Gandara-Rey J. Mandibular nerve paresthesia caused by endodontic treatment. Med Oral. 2003;8(4):299-303.
- Blanas N, Kienle F, Sandor GK. Inferior alveolar nerve injury caused by thermoplastic gutta-percha overextension. J Can Dent Assoc. 2004;70(6):384-7.
- Gatot A, Tovi F. Prednisone treatment for injury and compression of inferior alveolar nerve: report of a case of anesthesia following endodontic overfilling. Oral Surg Oral Med Oral Pathol. 1986;62(6):704-6.
- Girard KR. Considerations in the management of damage to the mandibular nerve. J Am Dent Assoc. 1979;98(1):65-71.
- Becker KW, Kienecker EW, Dick P. A contribution to the scientific assessment of degenerative and regenerative processes of peripheral nerve fibers following axonotmesis under the systemic administration of vitamins B1, B6 and B12--light and electron microscopy findings of the saphenous nerve in the rabbit. Neurochirurgia (Stuttg). 1990;33(4):113-21.
- Unlu E, I Ergin, O Besalti, O Koskan, Z Pekcan. The contribution of thiamine, pyridoxine and cyanocobalamine combination on nerve regeneration in rats with experimentally induced sciatic injury. J Anim Vet Advances. 2007;6(2):4.
- Queral-Godoy E, Valmaseda-Castellon E, Berini-Aytes L, Gay-Escoda C. Incidence and evolution of inferior alveolar nerve lesions following lower third molar extraction. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2005;99(3):259-64.
